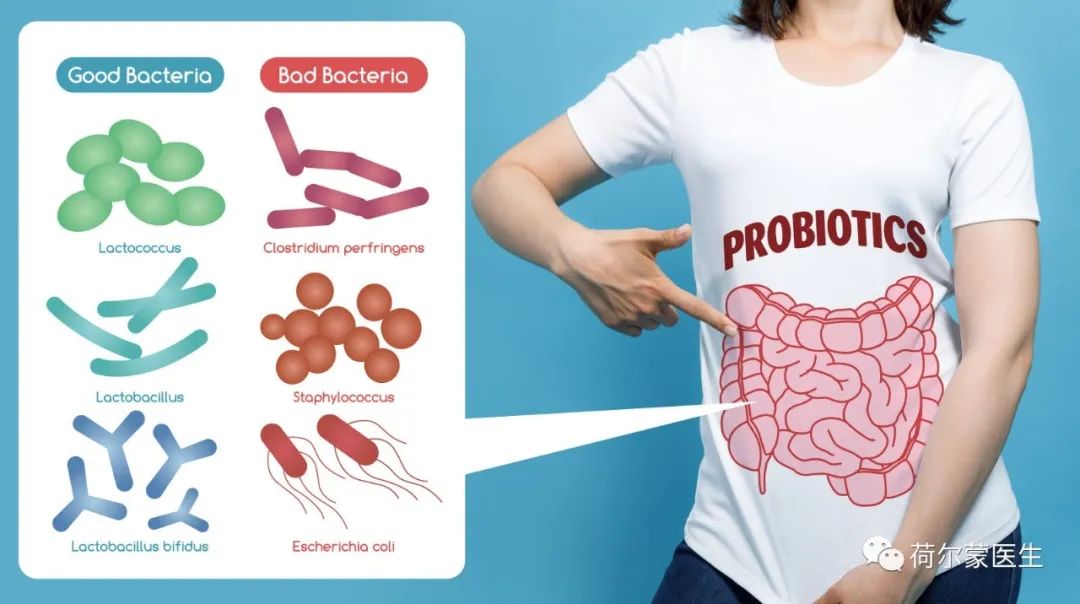


肠道菌群是人体胃肠道系统内一个数目庞大的微生物有机群体。近年发现,肠道菌群参与人体心血管、内分泌与代谢等系统生理功能的调节。甲状腺是人体内分泌系统的重要调节器官。碘离子是甲状腺激素分子结构中重要的构成元素;同时,微量元素硒在甲状腺激素T4向T3的转化中起到必不可少的作用。肠道菌群的组成结构异常,不仅参与了自身免疫性甲状腺疾病的免疫调节,而且影响甲状腺激素相关物质如外源性甲状腺素、碘以及硒元素的吸收和代谢,进而影响甲状腺稳态。
肠道菌群是寄生在胃肠道的微生物有机群体的重要组成部分,数目庞大,它们和少量的真菌及病毒等,共同构成人体胃肠道的微生物有机体。动物实验证实,肠道菌群参与维持胃肠道系统的免疫抑制及炎性反应间的动态平衡,其中涉及Toll样受体相关信号通路。另有临床报道称,溃疡性结肠炎患者可伴随继发性弥漫性甲状腺淀粉样变。甲状腺是人体最大的内分泌调节器官,它与肠道菌群间是否有某种关系,它们是否相互影响?


01
肠道菌群的形成及分布


从脱离母体之日起,人体肠道已经开始有细菌驻入并生长。在长期的饮食习惯、遗传及环境条件作用下,肠道菌群和宿主之间维持着动态平衡;然而,一旦发生饮食习惯巨大改变、外源性病原体入侵、抗生素不适当使用等,菌群与人体之间的动态平衡将受到干扰。在胃肠道,结肠菌群分布最多,约10¹⁴CFU/ml( colony-forming units/ml);空、回肠其次,约10⁴ - 10⁸ CFU/ml;胃和十二指肠分布最少,约10³CFU/ml。


02
肠道菌群与甲状腺稳态之自身免疫
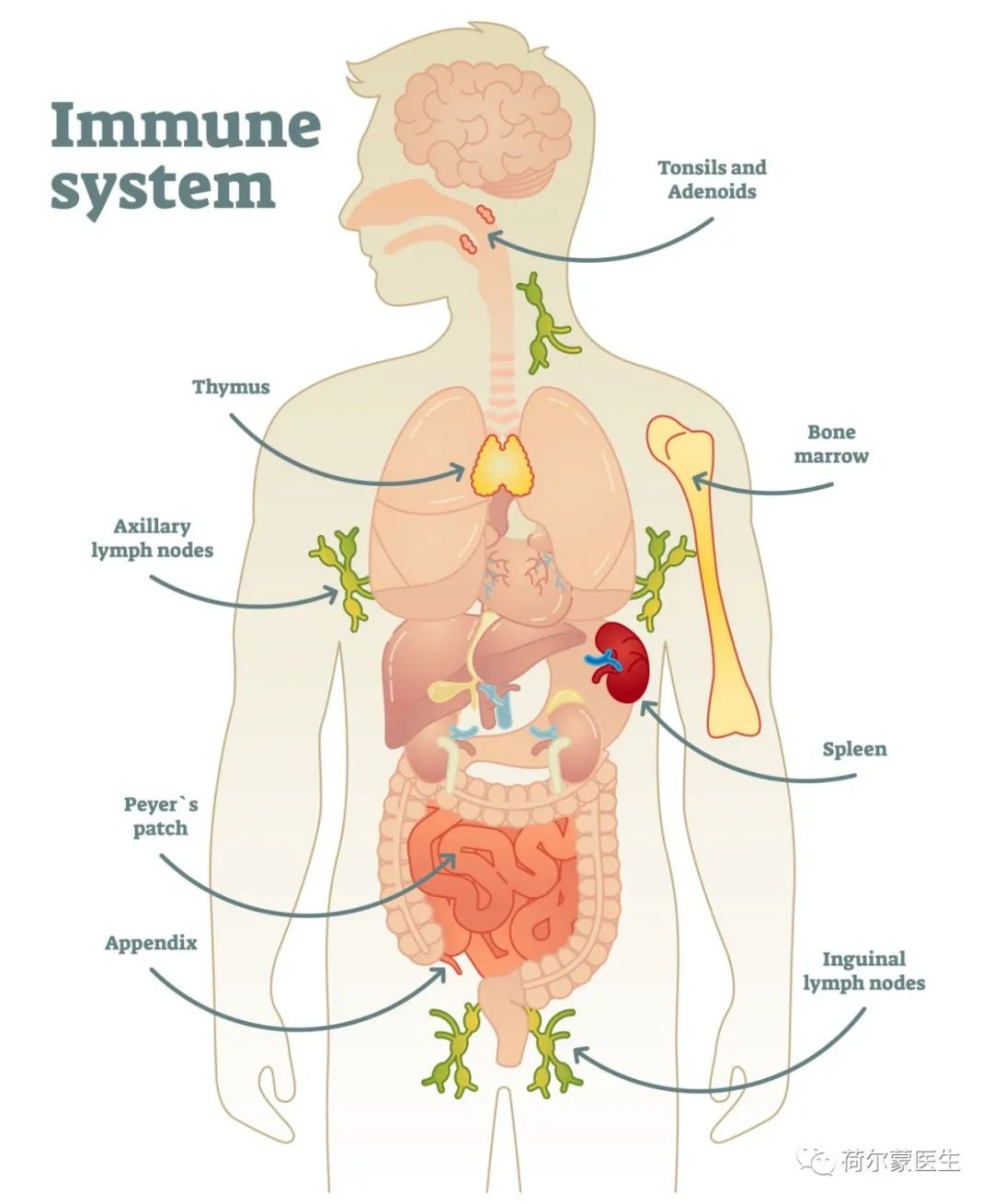


桥本甲状腺炎是自身免疫性甲状腺疾病中较为常见的一种,它是一种器官特异性自身免疫性疾病, 通常由遗传和环境因素共同作用而诱发。它以甲状腺组织中单核细胞浸润以及抗甲状腺球蛋白抗体和 抗过氧化物酶抗体为疾病特征。环境因素中,饮食中碘摄入与桥本甲状腺炎的关系受到广泛关注。另有研究报道,肠道中厌氧菌可干扰2,4,6 碘代苯衍生物的脱碘环节,提示肠道菌群与桥本甲状腺炎之间可能存在某种关联。然而,相关发现目前只呈现冰山一角,更多的现象及机制有待进一步研究。
非肥胖糖尿病鼠NOD.H2h4是一种自发的自身免疫性甲状腺疾病模型。和人类自身免疫性甲状腺炎极为相似,NOD.H2h4小鼠甲状腺组织中有标志性的单核细胞浸润,含有CD4.CD8细胞。另有文献报道,该模型鼠甲状腺中亦含B细胞、巨噬细胞、树突状细胞等。在绝大多数实验中,NOD.H2h4小鼠被饲养在SPF级别环境。在一项研究中,一组该品种小鼠被养于SPF级别饲养笼,另外一组相同品种小鼠被养于普通饲养笼,研究者发现,普通饲养笼里部分小鼠在20周龄时即出现自身免疫性甲状腺炎,40周龄时所有该普通饲养笼中小鼠均出现一定程度的甲状腺疾病,并且回归分析显示,随着周龄增加,该组小鼠甲状腺炎严重程度增加 (R²=0.44)。而饲养在SPF级别笼中的小鼠直到30-39周龄才出现甲状腺疾病。该组小鼠随着周龄增加,甲状腺疾病患病数量呈缓慢增加,并且在39周龄时,相对于普通饲养组,该SPF组小鼠年龄与甲状腺疾病严重程度相关指数(R²=0.05)远低于普通饲养组小鼠。在普通饲养笼中的NOD.H2h4小鼠比在SPF饲养环境下的同种小鼠更可能出现自身免疫性甲状腺炎。
自身免疫性疾病是以免疫反应介导的组织破坏和功能损伤为特征的疾病,这和致病原介导的感染过程类似。活细菌以及它们的组成部分和代谢产物都与这些免疫机制相关。
关于自身免疫性疾病,人们一直在努力探究其导致自身免疫耐受缺失的机制。微生物感染通常被认为是先天遗传易感个体发生自身免疫性疾病的诱发因素。一个基于免疫交叉反应,又叫“分子模拟”的假设理论,可以解释感染因素如何导致自身免疫反应。“分子模拟”是指自身抗原与环境中某种抗原物质在抗原决定簇上存在相似性。另外,感染因素也可通过先天免疫细胞的不适当反应来诱发自身免疫性疾病。细菌的某种组成成分或许参与了抗原递呈细胞如树突状细胞的激活,从而导致自身抗原的暴露。小鼠和人类肠道所含的免疫球蛋白分泌细胞,比任何淋巴器官都要多,是人体免疫系统的重要组成部分。肠道黏膜表面寄居着各种食物抗原、细菌病原体以及各种互惠共生的细菌群体,它们共同维持着肠道的微环境稳态并防止着外来物质通过黏膜层入侵机体。
事实上,已有报道菌群的改变与炎性肠病或 1型糖尿病相关,它可诱发以上疾病自身免疫的启动。然而,肠道菌群如何参与自身免疫性甲状腺疾病的发病尚不得而知。


03
肠道菌群与甲状腺稳态之硒代谢


乳酸菌是人体肠道内极为重要的菌属,主要包括乳酸杆菌、肠球菌、链球菌等。肠道乳酸菌群可提高人体细胞内多种微量元素浓度,如硒元素等。硒是参与甲状腺激素代谢的重要微量元素。甲状腺腺体本身富集了人体绝大多数的硒。体内硒的含量和状态将影响机体甲状腺激素代谢。硒元素可参与甲状腺激素活化形式的转换,并能保护甲状腺腺体本身免受激素合成过程中氧化反应的损伤。
另有研究指出,当肠道菌群对硒亲和力增加,将影响宿主对硒的充分利用,影响含硒蛋白的合成,进而影响体内脱碘酶的合成。然而,当体内硒含量充沛时,这种竞争是否对人体造成生理学影响,还不得 而知。


04
肠道菌群与碘化甲腺原氨酸代谢


碘化甲腺原氨酸可通过多种途径代谢,其中,通过脱碘酶代谢是最主要的途径。脱碘酶包括1型、2 型和3型脱碘酶。1型脱碘酶主要表达在肝脏、肾脏和甲状腺,2型和3型脱碘酶主要发现于中枢神 经系统。早前有研究称在大鼠肠道探测到2型和3型脱碘酶活性,并且,幼鼠体内多于成年大鼠,作者推而此现象归因于成年大鼠肠道菌群较幼鼠更强的抑制作用。而后,人体肠道内也发现了脱碘酶活性。研究者推测,由于肠道有广泛的接触面积,其与体内三碘甲腺原氨酸池也许存在相关关系。进一步推测,碘化甲腺原氨酸的其他代谢通路似乎也与肠道菌群有关。在肝脏,葡糖醛酸化和硫酸化共轭在碘化甲腺原氨酸代谢中起主要作用。硫酸化作用使脱碘酶失活,而葡糖醛酸化作用提供大量的共轭甲状腺素,后者通过胆汁分泌进入肠道。以此看来,肠道细菌可能在很大程度上影响着酶活性,肠道菌群的组成将参与影响甲状腺代谢平衡关键通路。已有研究证实,大鼠和人体肠道粪便沉渣可大量水解碘化甲腺原氨酸轭合物,原因正是由于肠道内存 在着专性厌氧菌,而它们是肠道菌群正常组成部分。事实上,大多数的葡糖醛酸酶活性是和细菌有关的。所以,肠道菌群参与了碘化甲腺原氨酸的代谢。


05
肠道菌群与外源性甲状腺激素的吸收


口服甲状腺素是治疗各种原因导致的甲状腺功能减退症患者的常用治疗药物。肠道菌群通过影响胃肠屏障系统的结构及功能完整性,从而影响外源性甲状腺激素的吸收,进而影响甲状腺的功能状态。
已明确的是,上消化道功能紊乱和肠道菌群结构改变有关。同时伴随机体甲状腺素需要量的增加。乳糜性肠病患者较正常人肠道内乳酸菌及双歧杆菌数量减少,而这两种菌属中的某些菌种可以保护肠道上皮细胞免受麦胶蛋白相关肠黏膜损伤。尽管目前尚缺乏有关不同肠道菌群结构与甲状腺素吸收相关的实验研究,但已明确,乳糜性肠病和乳酸不耐受患者存在甲状腺素的吸收不良。这表明肠道菌群的组成结构异常参与形成了药物吸收不良的出现。近期有研究报道,在胃酸不足患者中存在着肠道菌群失调。这也许与萎缩性胃炎患者中,甲状腺素的需求量增加有关网。尽管患者甲状腺素的药物需求量增加主要与胃内酸碱度有关,但是不能不怀疑,菌群失衡也许是导致外源性甲 状腺激素吸收不良的原因之一。


06
小结


目前,肠道菌群与甲状腺稳态之间相关研究还仅呈现冰山一角。如前文所述,上消化道系统对甲状腺内源性和外源性激素的合成代谢起关键作用, 至于所涉及的具体菌属,相关研究不甚明了;免疫学研究目前是各系统疾病病因学及遗传学研究的热点,针对肠道菌群与疾病免疫,相关领域呈现出巨大的研究空间。自身免疫性甲状腺疾病是人类免疫系统疾病的重要组成部分,充分发掘肠道菌群对该系统疾病的作用机制,将为内分泌常见甲状腺疾病的诊疗提供新的思维视角。



