
新毒株的出现,让大家的心又慌了起来:没阳的怕阳了,阳了的又怕二次感染。
除了自身免疫力,抗衰老学家还发现了一个会影响我们感染几率的关键,那就是端粒。
一项美国与意大利合作开展的研究发现,端粒缩短或损伤导致的端粒功能障碍,会提高肺部血管紧张素转化酶2(ACE2)的表达,它是新型冠状病毒SARS-CoV-2的受体,它的表达提高会致使新冠感染风险大幅增加[1]。研究人员认为这解释了为什么老年人更容易感染新冠。该论文发表在顶级国际期刊EMBO reports上。


众所周知,衰老与癌症、心血管疾病、阿尔茨海默症等诸多疾病有着千丝万缕的联系,而SARS-CoV-2病毒作为冠状病毒界的新晋顶流,与衰老之间更是剪不断理还乱。
一方面,衰老是影响新冠感染的关键因素。中国疾病控制与预防中心的报告显示,40岁以下的感染人群死亡率仅为0.4%,但80岁以上的老年人死亡率却高达14.8%,整整提高了37倍[2]。美国疾病控制与预防中心的报告也发现,老年人感染后的住院率、重症病房收治率及死亡率远高于年轻人[3]。
这些数据无不表明,新冠更“偏爱”老年人。

此外,一些用于延缓衰老的药物和治疗方案,在新冠的治疗中异军突起。例如,顶级科研期刊Science就曾刊登一篇论文,指出清除衰老细胞可以使感染新冠的老年小鼠死亡率降低50%[4]。而二甲双胍在人体实验中表现也毫不逊色,直接使新冠患者的住院死亡率降低近4倍[5]。
如果一个疾病看起来像老年病,治起来也像老年病,那它就是老年病了。因此,新冠和衰老中间的关系,基本上是可以实锤的。

理清了新冠和衰老之间的关系,科学家不禁对其背后的机制产生了好奇,一番查探之后,血管紧张素转化酶2(ACE2)便进入了我们的视野。
ACE2,是许多细胞膜表面存在的一种蛋白质,能够调节血压、伤口愈合和炎症等过程[6]。然而,在新冠感染过程中,它却扮演了一个“带路党”的角色,不但不奋力反抗,反而开门揖盗:SARS-CoV-2病毒正是通过与ACE2结合才得以进入细胞[7]。因此,ACE2的表达水平,在新冠感染中可以说至关重要的。
实验中,研究人员发现随着年龄增长,肺部细胞的ACE2表达不断提高,因此更多SARS-CoV-2病毒有机会进入细胞,导致感染新冠的风险大幅增加。这或许能解释为什么老年人更容易感染新冠。
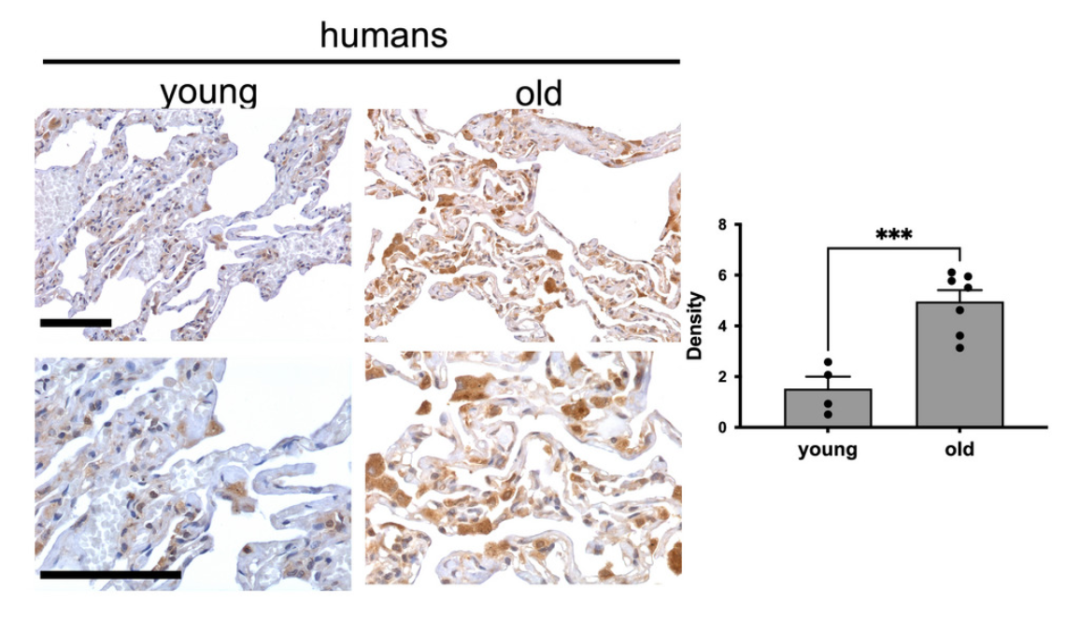
图注:年轻人(20-35岁)和老年人(60-80岁)肺部ACE2免疫组织染色对比
那是什么促使ACE2表达随衰老而增加?答案又绕回到我们熟悉的端粒缩短和损伤上。
实验中,为了探究端粒缩短对ACE2表达的影响,研究人员使人成纤维细胞和人支气管上皮细胞群体倍增,然后对细胞中ACE2的mRNA水平进行测量。结果显示,与早期传代、端粒较长的细胞相比,晚期传代的细胞端粒较短,ACE2的mRNA表达也显著增加。这表明端粒缩短会提高ACE2水平。
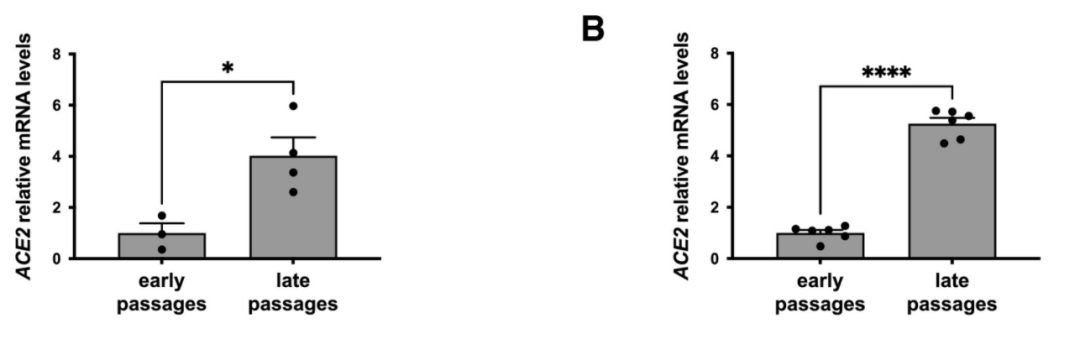
图注:人成纤维细胞(左)和人支气管上皮细胞(右)早期和晚期传代细胞ACE2的mRNA表达
之后,研究人员又在端粒未缩短的情况下,敲除了抑制端粒DNA损伤修复(DDR)通路的基因,从而探究端粒损伤和ACE2的关系。结果显示,端粒损伤会激活DDR通路,ACE2表达也随之水涨船高。
也就是说,在衰老过程中端粒累积的缩短和损伤,都是通过激活DDR通路来改变SARS-CoV-2病毒受体ACE2的水平,从而提高新冠感染风险。

既然已经知道了端粒、ACE2和新冠的作用机制,我们自然就要想办法抑制它们。
端粒反义寡核苷酸,是一种分子药物,通过靶向功能失调的端粒的tncRNA,减少激活DDR通路过程中必不可少的端粒DNA损伤。研究人员发现,使用端粒反义寡核苷酸对小鼠进行腹腔注射,一段时间后小鼠体内的ACE2表达与对照组相比显著减少,证明了该疗法的有效性。
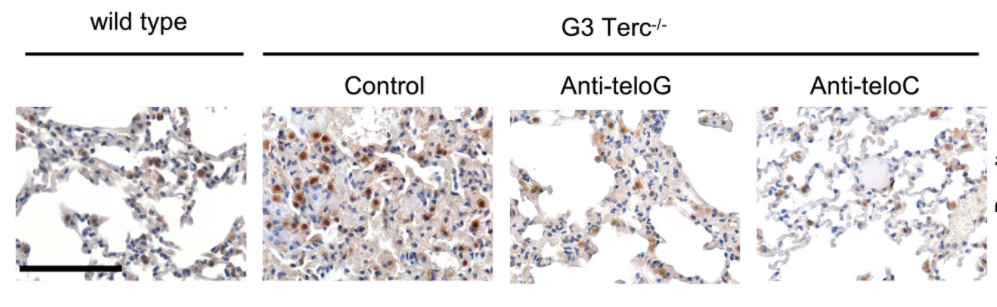
图注:野生、对照、两种反义寡核苷酸治疗小鼠体内ACE2免疫组织化学染色对比
因为目前反义寡核苷酸已经被批准用于治疗多种疾病,因此如果有更多实验能进一步证实它对新冠相关疾病的影响,它很快就能够作为一种新冠治疗药物用于临床试验中,在疫情中出一份力。
时光派点评
TOP期刊、端粒、衰老、新冠,诸多要素齐聚,为我们抗击新冠指明了一个新的治疗思路。
不得不说衰老就是个圈,哪怕是新冠这样棘手的传染病,一旦与衰老沾上关系,兜兜转转之后不免又要回到我们熟悉的抗衰上:要想抗击新冠,就要减少ACE2表达;要想减少ACE2表达,就要减少端粒缩短和磨损;要想减少端粒缩短和磨损,就要延缓衰老。
但无论抗衰药物在实验中表现出了多么优异的疗效,在它们被纳入新冠治疗指南前,都只是“锦上添花”,只能作为预防手段之一。
因此,在与新冠疫情的长期“斗争”中,保护端粒、延缓衰老是我们极其需要注意的,但除此之外口罩还得戴,疫苗还得打,医生的话还得听。

国际抗衰服务管理中心
—— TIMEPIE ——

参考文献

