
编者按
此前,我们曾引用皮肤病学家的美容食谱,从皮肤衰老的角度,为大家介绍过糖化反应与晚期糖基化终末产物(AGEs)在衰老当中所扮演的角色,并且给出了一些实际可行的“抗糖”小妙招。(原文链接:吃糖一口,加速变丑——皮肤糖化与抗糖饮食)
这一次,我们为大家带来一篇发表于顶尖学术刊物《细胞代谢》杂志的综述。这篇综述详细阐述了晚期糖基化终末产物(AGEs)如何促进衰老、引发衰老相关疾病的机制。文章通讯作者Pankaj Kapahi教授长期致力于研究营养信号和代谢在衰老和衰老相关基本中的作用,着眼的工作重点之一正是经典的糖化理论。1912年,美拉德发现晚期糖基化终末产物(AGEs),它就在冥冥之中和“衰老(ageing)”结下了不解之缘;1980年代,Monnier和Cerami提出美拉德衰老理论,假设AGEs的缓慢、持续积累是衰老的一个重要原因;时至今日,关于AGEs是衰老的因还是果,却仍然存在着争论……



晚期糖基化终末产物(AGEs)不是某种单一的物质,而是一组异质分子,但它们具有一些共同的特点:由美拉德反应(褐变)生成、荧光性、交联性、不溶性、随着年龄增长在胶原蛋白和晶状体蛋白中的累积增加。
这些化合物的长期累积可能会改变蛋白质的结构和功能,从而影响衰老的几个生物标志,也可能导致糖尿病和动脉粥样硬化等代谢相关的病理过程,以及引发与神经退行性疾病相关的氧化应激与炎症。
No.1
AGEs有两个来源
AGEs的两大来源之一是内源性生成:AGEs是由细胞或长寿命的细胞外蛋白通过糖化作用产生的。蛋白质糖化是一系列复杂的连续反应,统称为美拉德反应,组织和体液中显著浓度的葡萄糖、果糖或其他二羰基化合物均可与蛋白质发生美拉德反应。
在慢性高血糖扰动机体正常代谢和生化反应的状况下,一些由无氧糖酵解和脂质过氧化作用产生的副产物——α-二羰基化合物(α-DC)的水平会显著升高,α-DC发生糖化反应的反应性远远强于葡萄糖,它们能无差别地与蛋白质、脂质和DNA反应形成AGEs。甲基二乙醛(MGO)是一种α-DC,它在糖酵解过程中从磷酸丙糖异构体产生,是形成AGE是的关键前体。MGO之类的高反应性AGE中间体,也被一些学者命名为糖毒素(glycotoxin)。
AGEs的另一个重要来源是食物在烹调过程中产生,尤其是经干热烹调的食物,通过食物摄入被人体吸收。

No.2
肾脏是排泄AGEs的关键器官
已经产生或吸收的AGEs人体不能通过酶促反应将其分解,血液循环中部分水解的AGE-肽和游离的AGE加合物可在肾脏被滤过而后排泄;人和大鼠肾脏的AGEs-肽清除率低于肌酐清除率,这说明肾脏对于AGEs除了滤过还有一部分重吸收作用。
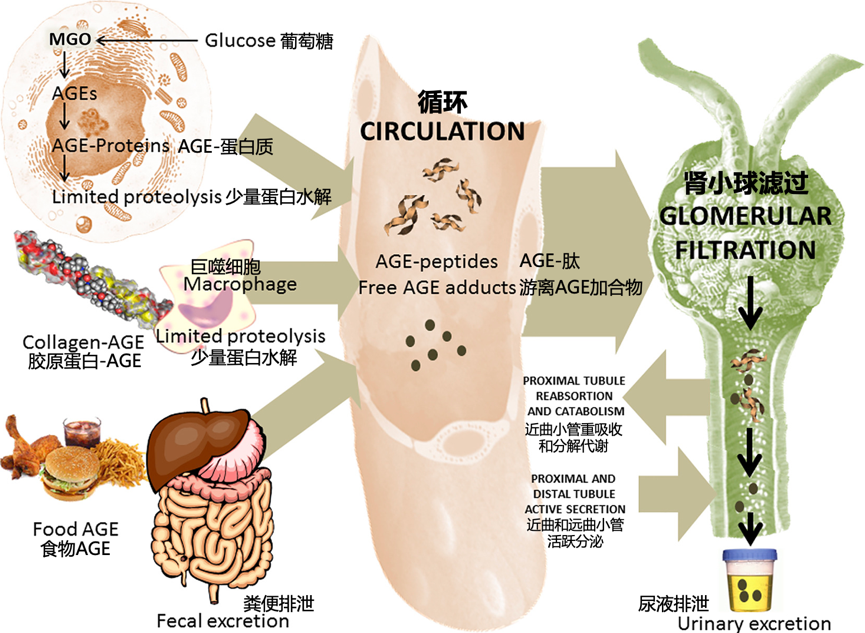

大量证据表明AGEs在多个物种的衰老过程中累积,AGEs造成胶原蛋白交联及其与动脉疾病的关系,是导致糖尿病并发症和加速衰老的主要原因之一,已经成为了科学界共识。
根据一项针对65岁及以上人群的研究发现,血浆中高羧甲基赖氨酸(一种AGE)水平,与老年人全因死亡率及因心血管疾病导致的死亡风险增加呈正相关;有趣的是,研究还发现羧甲基赖氨酸水平升高与死亡风险增加的关联,与糖尿病无关。因此,AGEs可能不仅仅是一种生物标志物,还是衰老的潜在驱动因素。
基于人体的研究证据虽有启发性,但结果仅仅是具有相关性。AGEs与寿命之间存在直接因果证据的研究来自对秀丽隐杆线虫的研究。比如,高葡萄糖条件下,线虫体内乙二醛酶GLOD-4功能丧失,会加剧二羰基化合物介导的AGEs对线粒体蛋白的修饰,也会缩短线虫寿命;对线虫施用抗结核药物利福平,可减少与年龄相关的AGEs积累,通过激活DAF-16/FOXO延长线虫寿命。
此外,在8种哺乳动物中进行的研究验证,皮肤样本中AGEs的积累速率与最大寿命成反比。目前有大量证据可证实AGEs在衰老过程中发挥着作用,并同衰老速率有因果关联。

No.1
糖尿病相关并发症
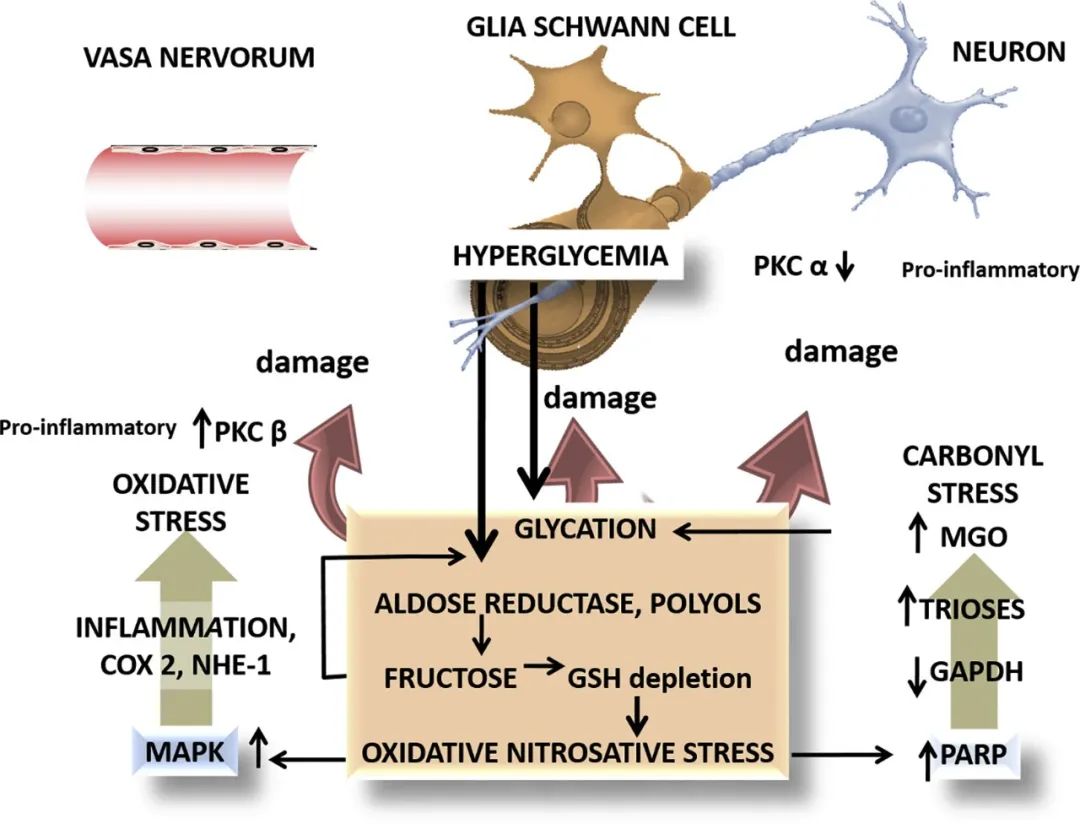
糖尿病中长期的高血糖会导致多种病症,统称为糖尿病并发症,包括周围神经病变、心肌病、肾病和视网膜病。对糖尿病并发症的分子病理基础最有说服力的解释之一,是葡萄糖分解代谢衍生的反应性副产物α-DC的积累。
AGEs 通过作用于神经血管、神经元和神经胶质细胞,对神经造成三重打击;AGEs也通过促进纤维化等机制引发糖尿病肾病;AGEs还通过损伤血管内皮细胞,诱发级联炎症反应和血管功能障碍,导致糖尿病相关微血管和大血管疾病。
除了内源性途径积累的AGEs以外,饮食来源的外源性AGEs同样对相关疾病有显著影响,喂食小鼠高AGEs的饲料后,小鼠出现非酒精性脂肪性肝病(NAFLD)的病理特征,除了体重增加,脂肪组织还分泌了大量炎症因子。这与西方饮食(也是AGEs的主要来源)的影响一致,是导致胰岛素抵抗的慢性炎症和氧化应激背后的致病因素。
No.2
神经退行性疾病
除了糖尿病并发症外,AGEs还会导致与年龄相关的神经变性。
当喂食小鼠高升糖指数(GI)的饮食时,脑内AGEs形成显著增加,且主要发生在黑质中,这是帕金森病(PD)的主要病理特点。关于AGEs和PD发病机制的研究,也解释了为何糖尿病患者患帕金森病的风险显著增高。
除PD外,AGEs还与阿尔茨海默症(AD)相关。先前的研究表明,AD相关蛋白(如Aβ和tau)的糖基化在这种疾病的发病机制中起着关键作用。与年龄匹配的健康人脑相比,从AD患者大脑中提取的斑块显示AGE含量增加了3倍。此外,AGEs被认为可以稳定和促进聚集形式的Aβ和tau的形成。这些证据也有利于解释流行病学研究发现的2型糖尿病和AD发病之间的联系。

No.1
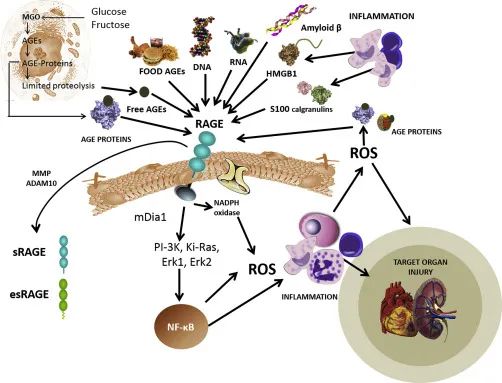
RAGE通路与氧化应激:AGEs参与慢性病致病的关键机制
AGEs是多种促炎和抗炎细胞受体的配体,其中一种关键的促炎受体是晚期糖基化终末产物受体(RAGE)。与配体结合后,RAGE启动信号级联反应,激活核因子-κB (NF-κB)、氧化应激和炎症。RAGE活性与糖尿病微血管并发症相关,包括糖尿病肾病、视网膜病和神经病。
No.2
AMPK:是MGO损害的关键目标吗?
MGO应激可能通过影响AMPK,与代谢疾病,尤其是代谢综合征相关。AMPK是调节细胞能量状态(激活分解代谢途径和抑制合成代谢途径),维持能量稳态的中央控制点。AMPK上的三个精氨酸残基是AMP的结合位点,这个变构位点容易受到羰基攻击,尤其是甲基二乙醛(MGO)。
AMP水平非常小的升高可以引起AMPK活性显著增加,这表明即使是最低限度的AMP变构位点阻断,也可以放大 AMPK 激活减少。AMPK的失活将增强脂肪生成、胰岛素抵抗和高血糖,这些都是代谢综合征和糖尿病的标志。体内果糖水平升高、高血糖和氧化应激所致甘油醛-3-磷酸脱氢酶(GAPDH)失活,均可能造成MGO通量增加。

氨基胍(可通过与α-DC相互作用降低AGEs水平)曾,进行过一项用以治疗糖尿病肾病人体临床试验,但不幸的是,由于其副作用,有关公司于1999年停止了对该药物的开发。
科学家们需要设计新的方法,通过利用适当的内源性防御降低AGEs,这可能会阻止AGEs 的形成,并造成更少副作用。在最近一项临床试验中,反式白藜芦醇(tRes)和橙皮素(HESP) 的联合疗法,通过诱导乙二醛酶(Glo1),改善了健康超重和肥胖个体的血糖水平和血管炎症。这表明通过诱导乙二醛酶,抑制MGO积累,是糖化介导疾病的潜在治疗策略。
乙二醛酶的表达和活性还受到核因子类胡萝卜素2相关因子2(Nrf2)的调节,它也可能成为减低AGEs水平、减轻糖化介导疾病的良好靶标。

国际抗衰服务管理中心
原文链接

